新闻中心
介质研磨法制备阿奇霉素纳米晶
作者:admin日期:2020-07-15阅读
采用介质研磨法制备了阿奇霉素纳米晶,考察了机器转速、研磨时间、氧化锆珠的大小及用量、表面活性剂的种类及浓度、阿奇霉素的浓度等因素对产品粒径及多分散指数的影响.分别采用扫描电镜(SEM)、粒度测定仪、x射线粉末衍射(XRPD)、红外光谱仪(FT—IR)对纳米晶进行了分析和表征,同时对纳米晶和原料药进行了溶出性能研究.实验结果表明,在优化的条件下,可制备平均粒径为165 am的阿奇霉索纳米粒子,研磨前后药物的晶态没有明显改变;与原料药相比,纳米晶的溶出度有了显著提高.
阿奇霉素(Azithromycin,AzM)是新一代大环内酯类,其谱广,不对革兰氏阳性球菌、、支原体、衣原体有作用,对一些革兰氏阴性菌,包括淋球菌、流感嗜血杆菌等也有较好的作用[].该药通透性高,溶解度,是典型的生物药剂学分类系统Ⅱ类药物,导致了其在人体中吸收不佳,生物利用度为37 ,降了疗效.解决这类问题的方法,通常是将药物制成可溶性盐类,改变晶型制成无定型药物,采用微粉化、固体分散体技术以增加药物的表面积,制成包合物等 ].
地质大学的王龙艳等[3 采用微粉化技术分别制备了平均粒径在1.0 m 左右的AZM 超微粉体,在一定程度上改善了阿奇霉素的溶解度和溶出度,但也存在制备方法能耗高、产品收率、易污染等一些问题.随着科学技术的不断进步,纳米化得到了普遍发展.由于比表面积急剧,将药物纳米化可以有效地克服难溶性药物生物利用度的问题,纳米药物伴随这种趋势应运而生[6].
地质大学的王龙艳等[3 采用微粉化技术分别制备了平均粒径在1.0 m 左右的AZM 超微粉体,在一定程度上改善了阿奇霉素的溶解度和溶出度,但也存在制备方法能耗高、产品收率、易污染等一些问题.随着科学技术的不断进步,纳米化得到了普遍发展.由于比表面积急剧,将药物纳米化可以有效地克服难溶性药物生物利用度的问题,纳米药物伴随这种趋势应运而生[6].
纳米药物是指结合纳米技术和药学理论,将药物制成粒径为1~1 000 nm 的载药粒子或纳米晶体[7],载药粒子一般包括纳米粒、纳米囊、纳米脂质体等,是基质骨架型或囊泡型纳米药物制剂,制备工艺复杂,载药量通常较[8 ;纳米晶体的研究始于2O世纪90年代,是一种“纯”的固体药物颗粒,含有少量稳定剂的胶态分散体系[9].目前,制备纳米晶的方法主要有介质研磨法、高压均质法、沉淀法、乳化法等.沉淀法和乳化法存在溶剂残留的问题;而高压均质法所需设备昂贵、能耗高.介质研磨法需将分散有药物的液体与研磨介质一起置于封闭的研磨室中,靠机器的运转带动药物粒子之间以及药物粒子与研磨介质、器壁间的撞击,
而达到纳米级~J,I E ].介质研磨法操作简单,生产成本廉,适合工业化大生产,采用该法已成功制备并上市了4种纳米晶制剂[1 .本文中,笔者以结晶型AZM 为原料。采用介质研磨法制备AZM 纳米混悬液,将混悬液冷冻干燥后,得到了颗粒均匀、粒度分布较窄、水再分散性良好的AZM 纳米晶.
1 试剂与仪器
1.1 试 剂
AZM 原料药、泊洛沙姆188(P188)、生育酚琥珀酸(TPGS,湖北恒硕化工有限公司);十二烷基硫酸钠(SDS,天津市大茂化学试剂厂);吐温80(天津市化学试剂三厂);乙腈、甲醇(色谱纯,Oceanp AK AlexativeChemical Compand,Ltd);其他试剂均为分析纯,实验室用水为双重蒸馏水.
1.2 仪 器
QM一3SP04行星式球磨机(南京大学仪器厂);Nano-$9O激光粒度测定仪(英国马尔文仪器公司);FTS一135傅里叶红外光谱仪(美国伯乐公司);S-4800-I冷场发射扫描电子显微镜(日本HITACHI公司);D/MAX一2500 X射线衍射仪(日本Rigaku公司);2010EV高效液相色谱仪(日本岛津公司);UV一2600紫外分光光度计(上海天美科学仪器有限公司);RCZ-8A药物溶出度测定仪(天津大学精密仪器厂)
2 实法
2.1 AZM 纳米晶的制备
准确称取一定量的表面活性剂置于100 mL的研磨罐中,加人15 mL的蒸馏水后超声2 rain.称取适量AZM 原料药置于上述研磨罐中超声数分钟,待药物充分分散后,加入一定量的氧化锆珠.安装机器,调节机器转速并运行球磨机.每2 h停机15 min,研磨一定时间后停机,静置一段时间,将所得混悬液冷冻干燥8 h,即可得到AZM 纳米晶.
2.2 纳米晶的表征
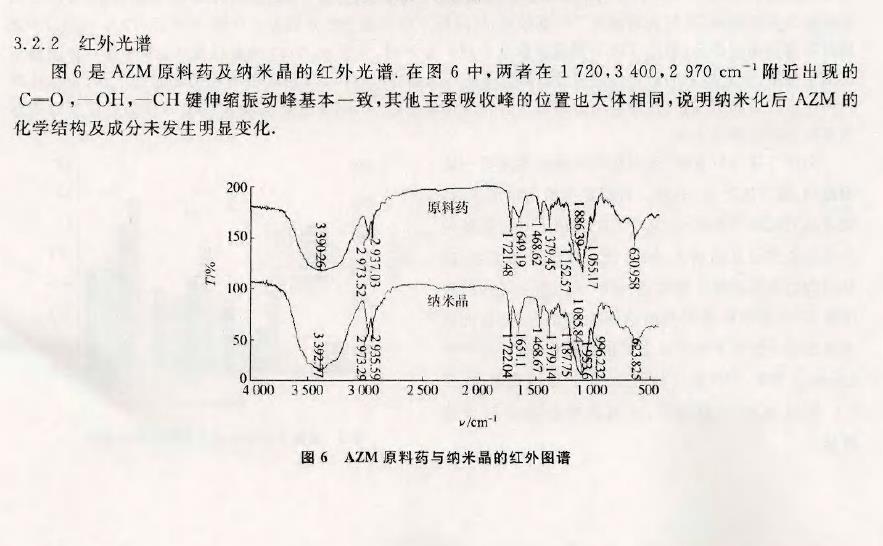
采用粒度仪测定AZM 原料药和纳米晶的颗粒粒径及分散性,并通过SEM 对其形态学进行确证;利用XRPD分析纳米晶的晶型特征;同时使用FT—IR在400~4 000 cm-1进行扫描,比较研磨前后药物化学结构
的变化情况.
2.3 溶出度实验
采用药典2010版(2部)[ 中溶出度测定法(附录XC2法),对ZAM原料药和优化条件下制备的纳米晶进行体外溶出度测定.将蒸馏水经脱气处理后,配制900 mL pH=1.0盐酸溶液作为溶出介质,搅拌桨转速设为100 r/min,水浴温度调节为37±0.5℃.待温度稳定后,分别向各溶出杯中投入样品,于1,2,3,5,7,1O,15,2o,3o,45,60 min取样5 mL,用0.22 m的微孔滤膜过滤,同时补加5 mL新介质.滤液经适当稀释,按药典2010版阿奇霉素项下含量测定法(HPLC法)测定其峰面积,计算溶出量并绘制药物的溶出曲线.
3 结果与讨论
3.1 影响因素的考察
考察了机器转速、研磨时间、氧化锆珠的大小及用量、表面活性剂的种类及浓度、AZM 的浓度等影响纳米晶粒径及多分散指数(polydispersity index,PI)的主要因素,以优化各实验参数,确定制备AZM 纳米晶的优条件.
3.1.1 机器转速
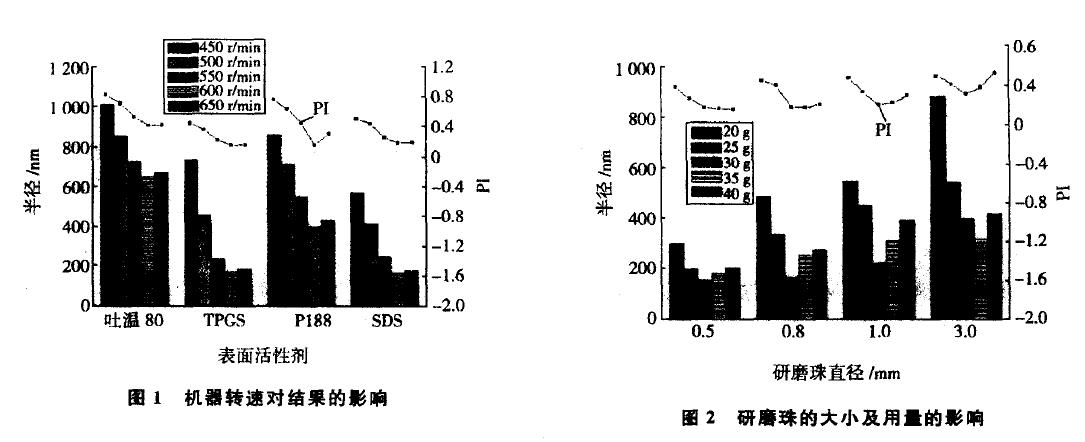
转速是研磨机的重要参数之一,决定着整个体系的动能.选择质量分数为5.0 (相对主药量)的不同表面活性剂,控制研磨时间为6 h,考察不同转速对产品的粒径及分散性的影响,结果如图1所示.从图1可以看出,在转速(450 r/rain)时,采用4种表面活性剂所制备的产品粒径均较大,PI值都大于
0.45,提示粒子的均一性不好,所得产品的粒度分布较宽;而随着转速的,颗粒的粒径不断减小,同时粒子的分散性也变好,尤其是采用TPGS作为表面活性剂,转速从450 r/min调到500 r/min时,所得产品的粒径减小近1倍;当转速达到600 r/min后,转速粒径不再减小,甚至有的趋势,除了使用P188的产品外,其余3种粒子的PI值基本不再变化.此外,在相同转速的条件下,采用TPGS和SDS作为表面活性剂的产品,其粒径都较小,同时粒子也分散得更均匀.因为在研磨过程中,药物粒子靠高速运转的球磨机产生的剪切力和氧化锆珠运动过程形成的挤压力作用而不断减小:在转速的情况下,体系没有足够的动能,使得药物粒子之间、粒子和氧化锆珠之间的碰撞效果较弱;而达到高转速时,产品粒径又开始,这可能是因为过高的转速使较小的粒子溶解后又析出,导致终产物颗粒粒径变大,或研磨前后体系温度的变化,导致这一过程的进行.综合产品粒径及PI的考察,机器转速的较优选择为600 r/min.
3.1.2 氧化锆珠的大小及用量
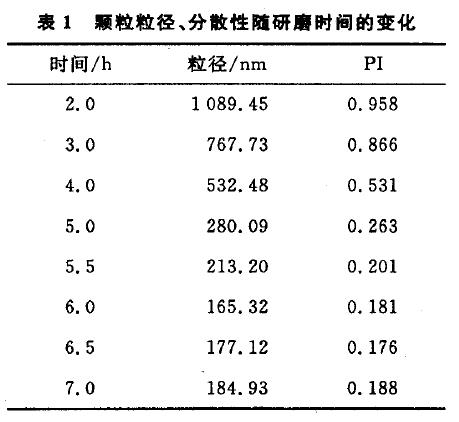
氧化锆珠是湿法研磨制备纳米晶的一个重要组成部分,药物大颗粒在氧化锆珠的挤压、碰撞下不断减小,因此选择合适大小及用量的氧化锆珠对实验的成功至关重要.实验选择了直径分别为0.5,0.8,1.0,3.0 mm的ZrO2珠,用量在20.O~4O.0 g,设定研磨时间为6 h,考察氧化锆珠对产品粒径及PI的影响,结果见图2.可知,当氧化锆珠粒径从3.0 mm改变到0.5 mm时,颗粒粒径也随之减小.这是由于珠子粒径越小,在同等数量下,其接触点和数量就越多,进而使药物和珠子之间的碰撞频率,提高了研磨效果.此外,当珠子粒径较小时,介质间隙可以起到过滤作用,将大颗粒截留并打碎,促进颗粒的减小,同时使得粒子的分散性变好.

从图2还可看到,为了得到较小的粒径,选择适量的研磨介质非常重要.图2中30 g(直径为0.5,0.8mm)珠子研磨所制备产品粒径分别为155,165 nm,PI值分别为0.175,0.181;而采用同等数量直径为1.0,3.0 mm 的氧化锆珠得到的粒径都较大(~-220 nm).对于每种粒径的氧化锆珠,纳米晶粒径都随着氧化锆珠用量的增多而逐渐减小,当超过一定用量之后,粒径又呈现的现象.这是因为研磨罐中含较少量的氧化锆珠时,接触点的数量减少;而用量时,在机器提供相同动能的情况下,氧化锆珠的撞击力度减弱,因此都达不到较好的研磨效果.实验中同时发现,小粒径的氧化锆珠(直径0.5 mm)虽然能制备出较小粒径的纳米晶,但产品不易与氧化锆珠分离且制备过程中氧化锆珠的损失较多,故选择30 g直径0.8 mm的ZrO。珠为宜.
3.1.3 研磨时间
称取30 g ZrO。氧化锆珠,选择SDS为表面活性剂,AZM 质量浓度为300 g/L,控制研磨时间在2.O~7.0h内,表1反映了产物粒径随研磨时间的变化规律.可见,随着研磨时间的延长,产品的粒径和PI值都明显减小,特别是在研磨初期,这种减小的趋势更加明显;当研磨时间为6.0 h时,产品的平均粒径减为小,此时粒子的PI值也较小;此后再增加研磨时间,粒径反而呈现的趋势,PI值也具有同样的现象.这是由于较长的研磨时间,可以使药物大颗粒被充分剪切、撞击而破碎成小粒子,同时有助于表面活性剂吸附在药物表面,以获得相对稳定的体系,并使纳米粒子能够较均匀地分散在液相中;而当研磨时间过长,颗粒之间可能会相互连接生长[1引,以及研磨体系温度升高导致颗粒的聚集,进而影响了产品的粒径和分散性.因此,实验选择研磨时间为6.0 h较合适.
3.1.4 表面活性剂的种类及浓度
当微粒经研磨转变为纳米级后,特别是数纳米到数十纳米,此时纳米晶拥有巨大的比表面积,表面能急剧增加,若没有合适的稳定剂润湿其表面,粒子就会慢慢聚集形成二次颗粒,进而失去纳米晶所特有的物理、化学特性[1 .常用的稳定剂有表面活性剂和高分子聚合物,其中表面活性剂由于分散
后溶液黏度、在颗粒表面可发生多层吸附等优点,是经常选用的一类稳定剂.本实验控制AZM 质量浓度为300 g/L,筛选了P188,SDS,TPGS和吐温8O等4种表面活性剂,考察了它们的质量浓度(相对主药量)对AZM 纳米晶粒径及分散性的影响,结果如图3所示.
图3反映出采用TPGS和SDS时,产品粒径都在473 nm以下,佳用量时粒径可减小到165 nm,P188作为稳定剂的效果比前两者差,而用吐温8O作稳定剂,产品粒径小为表l 颗粒粒径、分散性随研磨时间的变化602 nm,同时纳米晶的PI值也较大.分析原因,P188和吐温8O为非离子型表面活性剂,其疏水基团与药物结合而形成空间位阻,使得粒子间距离变大以粒子的团聚.但实验发现在球磨机高速运转的过程中,吐温8O受到剧烈撞击作用易产生泡沫。了药物粒子的运动,这也是吐温8O较P188有更强的疏水作用,但所制备产品粒径和PI值却较大的主要原因.TPGS也是非离子型表面活性剂,具有更小的亲水亲油平衡值,因此药物表面吸附更多的TPGS就会越疏水,进而形成稳定分散的体系;同时TPGS溶液的黏度更小,因而与P188相比,采用TPGS制备的纳米晶粒径大幅减小.高浓度的TPGS研磨后体系成为膏状体,导致产品和氧化锆珠分离困难,也大地减弱了研磨效果,因此图3中质量分数分别为5.0 ,8.0 ,12.0 的TPGS均没有得到相应产品;但把TPGS质量分数减小到0.1 时,又发现AZM 的粒径变大.SDS是一种阴离子表面活性剂,它对体系的稳定作用主要依靠电荷所产生的静电排斥,当SDS吸附在药物表面上后,可以使药物得到适当的润湿,同时在静电斥力作用下达到动力学稳定[1引,图3结果也显示了SDS作为稳定剂时能够制备更小粒径的纳米晶.
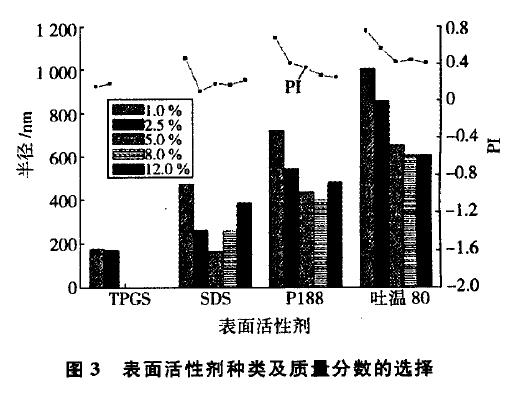


由图3还可以看到,表面活性剂的浓度也有一定的限制:除TPGS外,其他3种稳定剂的用量增多时,纳米晶的粒径不再减小,其中SDS和P188所制备的产品粒径甚至开始,同时分散性也开始变差.这是因为纳米晶的表面能大,使得粒子间相互碰撞的频率加大,以降体系而达到稳定状态.过量的表面活性剂会为粒子相互撞击提供架桥作用,从而产生Ostwald现象,加快粒子的团聚.实验结果表明,选择5.0 的SDS作为润湿、分散药物的稳定剂效果较佳.


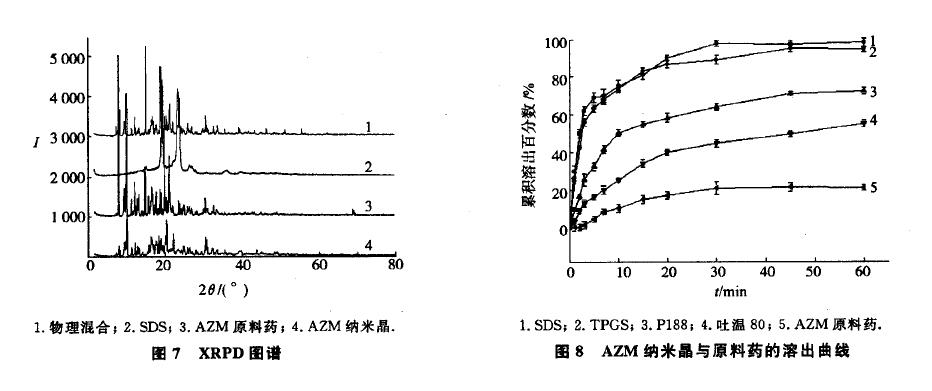
3.2.3 XRPD
AZM 原料药及纳米晶、SDS和同比例物理混合物的XRPD结果见图7.可知,原料药在7.94。,9.92。,14.68。,14.8O。,19.82。,20.96。处有尖锐的结晶衍射峰;而纳米晶和物理混合物图谱的2 在相应位置也有强烈的衍射峰,由于稳定剂的稀释作用,两者的峰强度与原料相比较弱.可见经研磨制备成纳米晶,其晶型并没有改变.
3.3 体外溶出性能研究
Noyes—Whitney方程常用于描述药物的溶出速度,粒径减小到纳米级别,药物的比表面积,进而加快药物的溶解,提高溶出度.实验研究了AZM 原料药与佳工艺条件制备的纳米晶(表面活性剂分别为SDS,TPGS,P188和吐温80)的体外溶出性能,溶出曲线见图8.可见,AZM纳米晶的溶出速率明显,在投样10 rain时,以SDS为表面活性剂的纳米晶的累积溶出率可达到75 ,是同一时间原料药溶出量的7.5倍左右;在45 min时纳米晶可基本完全溶解,而同一条件下原料药平衡时的溶出总量为21 左右.此外,图8也显示出不同表面活性剂所制备出产品溶出性能的差别,SDS和TPGS的产品在60 rain时溶出总量超过90 ;而P188和吐温8O的产品分别为72.5 ,55.1 ,并仍呈现上升趋势,这也充分说明减小粒径可提高AZM 的溶出性能.

4 结论
采用介质研磨法制备了AZM 纳米混悬液,并经冷冻于燥得到纳米晶.在研究过程中,考察了机器转速、研磨时间、氧化锆珠的大小及用量、表面活性剂的种类及浓度、AZM 的浓度等因素对纳米晶粒径及分散性的影响.终确定的佳工艺条件是:以质量分数5.0 0/G的SDS作为稳定剂,AZM 的质量浓度300 g/L,蒸馏水体积15 mL,30 g(直径0.8 mm)为氧化锆珠,转速为600 r/min,研磨总时间6.0 h.制备出的纳米晶呈较规则的长方体形,平均粒径165 nm,粒度分布在100~300 nm 内.经XRPD和FT—IR结果分析,该法制备的产品仍为结晶型AZM,化学结构没有变化;溶出度实验结果表明,AZM 纳米晶的溶出速率及溶出总量都较原料药有了明显改善.该方法制备过程简单,成本,产品的粒径小,分散性良好,有较好的应用前景.




